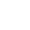Definice pH metru
pH metr je přístroj používaný ke stanovení hodnoty pH roztoku. pH metr pracuje na principu galvanické baterie. Elektromotorická síla mezi dvěma elektrodami galvanické baterie je založena na Nernsově zákonu, který se nevztahuje pouze na vlastnosti elektrod, ale také na koncentraci vodíkových iontů v roztoku. Mezi elektromotorickou silou primární baterie a koncentrací vodíkových iontů existuje odpovídající vztah a záporný logaritmus koncentrace vodíkových iontů je hodnota pH. pH metr je běžný analytický přístroj, který se široce používá v zemědělství, ochraně životního prostředí a průmyslu. Hodnota pH půdy je jednou z důležitých základních vlastností půdy. Při měření pH je třeba vzít v úvahu faktory, jako je teplota a iontová síla testovaného roztoku.
Princip pH metru
Hodnota pH je definována jako záporný logaritmus koncentrace vodíkových iontů ve vodném roztoku. I když to zní složitě, velmi jednoduše řečeno je pH číslo používané ke kvantifikaci kyselosti nebo zásaditosti roztoku. Číslo udává počet vodíkových iontů, které může specifická látka v roztoku uvolnit. V rozmezí pH je hodnota pH 7 považována za neutrální. Roztoky s pH 0–7 jsou považovány za kyselé a roztoky nad 7 až 14 se nazývají alkalické roztoky. V biologických systémech je hodnota pH kritická. Díky pečlivě nastavenému pH může většina biomolekul v našem těle plnit vynikající funkce. I v experimentálním systému musí být pro dosažení přesných výsledků udržováno požadované pH. Proto se v biologických experimentech používá zařízení zvané pH metr k pečlivému sledování pH.
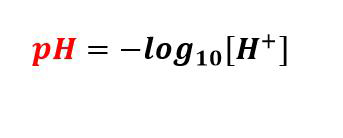
pH metr je elektroda citlivá na pH, která měří aktivitu vodíkových iontů v roztoku a přenáší tuto informaci. Zařízení se skládá ze dvou skleněných trubic, z nichž každá obsahuje elektrodu, referenční elektrodu a senzorovou elektrodu. Referenční elektroda je vyrobena z nasyceného roztoku KCl, zatímco senzorová elektroda obsahuje pufrovací roztok s pH 7 a stříbrný drát potažený chloridem stříbrným je ponořen do těchto dvou roztoků. Na konci senzorové elektrody je baňka vyrobená z porézního skla potaženého oxidem křemičitým a kovovou solí.
Pro měření pH roztoku se pH metr ponoří do roztoku. Poté, co se baňka senzorové elektrody dotkne roztoku, vodíkové ionty v roztoku nahradí kovové ionty na baňce. Tato substituce kovových iontů způsobí průtok proudu kovovým drátem, který se odečítá voltmetrem.
pH metr je jedním z nejpoužívanějších zařízení v biologických laboratořích. Pravidelně analyzujte pH pufrů, roztoků a činidel, abyste zajistili správné experimentální podmínky. Pro zajištění přesných měření je nutné zařízení pravidelně kalibrovat.
Použití detektoru pH metru
Aplikace pH metru v procesu čištění odpadních vod v domácnostech

Aplikace pH metru v elektrolytickém čištění odpadních vod

Aplikace online pH metru v průmyslu

Kalibrace pH metru
Čas zveřejnění: 15. prosince 2021